Tijdens de Internistendagen, die afgelopen week in Maastricht werden gehouden, kwam ik meerdere hele leuke wetenschappelijke studies tegen. Eén die me vooral opviel was die van de groep van prof. van de Poll-Franse uit Eindhoven (IKNL), uitgevoerd samen met o.a. het PHARMO instituut en met het Maxima Medisch Centrum. Zij vergeleken een grote groep van 3281 mensen met type 2 diabetes, bij wie tussen 1998 en 2011 een kwaadaardige aandoening werd vastgesteld, met 12891 controle personen met type 2 diabetes. Hierbij toonden zij aan dat díe mensen, die de diagnose alvleesklierkanker kregen, bijna VIJF keer zo vaak in de periode van 3 tot 6 maanden voorafgaande aan deze diagnose, een behandeling met insuline waren gestart. Ditzelfde gold ook voor maag-darm kanker (bron: abstractboek 27e Internistendagen, blz. 24-25).
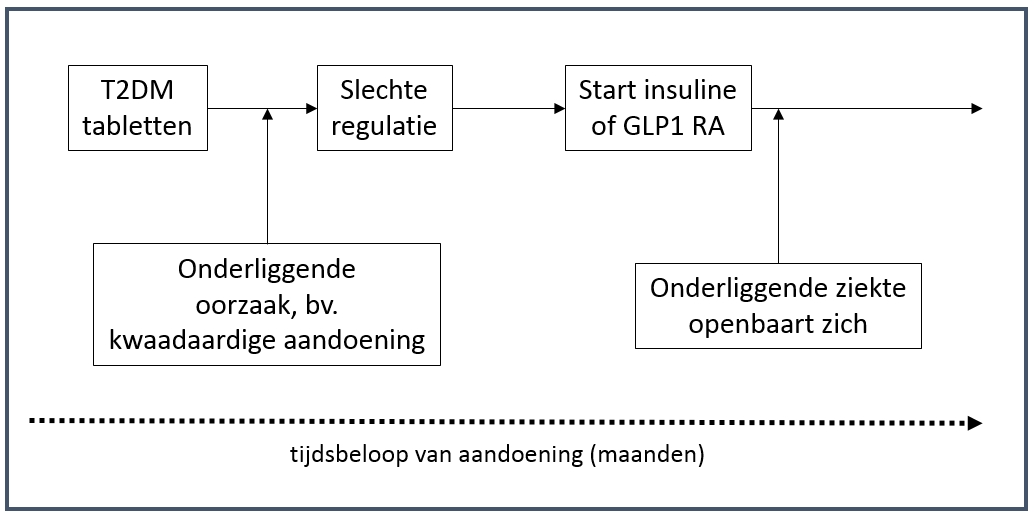
De onderzoekers gebruiken hiervoor dezelfde dataset als recent gepubliceerd in een interessant artikel in het gerenommeerde tijdschrift Diabetologia (http://www.ncbi.nlm.nih.gov/pubmed/25638246). Van de 3281 personen hadden er volgens hun beschrijving 387 (12%) slokdarm, maag, alvleesklier- of leverkanker. Zij geven aan dat er naar hun mening sprake is van ‘reverse causation’, dat wil zeggen dat de onderliggende ziekte (de kwaadaardige aandoening) de reden is voor de start van de behandeling met insuline, en niet andersom. Insuline therapie wordt immers gestart als de bloedglucose regulatie tijdens gebruik van tabletten verslechtert (zie figuur).
Melden bij Lareb
Stel nu dat u als dokter een patiënt behandelt, en die overzet op insuline, omdat de diabetes niet goed geregeld is, en die patiënt krijgt binnen 3 tot 6 maanden een kwaadaardige aandoening, dan is het heel goed mogelijk dat je dit meldt aan de bijwerkingeninstantie Lareb (www.lareb.nl). Een kleine blik in de publieke bestanden van Lareb leert echter iets heel anders. Wanneer we een groot aantal insuline soorten selecteren en tesamen beoordelen, te weten de insuline soorten actraphane, mixtard, actrapid, apidra, lispro, aspart, gewone insuline, glargine, en detemir, dan levert dit op dat TOTAAL welgeteld 8 x de bijwerking ‘neoplasmata’ is gerapporteerd, waarvan 2 keer de diagnose pancreasadenocarcinoom. Overigens suggereert de beschrijving van sommige meldingen dat er enkele doublures zijn: de bijwerking ‘pancreasadenocarcinoom’ wordt namelijk één keer gerapporteerd bij gebruik van insuline aspart en één keer bij gebruik van insuline detemir. Het zou mij niet verbazen als dit dezelfde melding is. Immers, patiënten gebruiken in de regel een snelwerkende insuline (aspart) en een basale insuline (levemir) tesamen.
Dit is van belang, omdat de afgelopen paar jaar kritisch wordt gekeken naar de risico’s van nieuwe medicijnen die op de markt komen. Met name GLP1 receptor agonisten (GLP1 RA) als exenatide en liraglutide worden nauwkeurig gemonitord als het gaat om bijwerkingen als pancreatitis en pancreaskanker. Van een middel als liraglutide is twaalf maal een melding van een neoplasma gedaan. Overigens dient iedereen hierbij zich te realiseren, zoals ook Lareb als disclaimer meldt, dat een melding die in de databank is opgenomen, niet hoeft te betekenen dat het verband tussen de klacht en het geneesmiddel vast staat, of dat überhaupt een causaal verband gesuggereerd kan worden.
Waarom wordt het vaststellen van kanker vlak na het starten van insuline niet gemeld?
Het feit dat nagenoeg nooit het optreden van een kwaadaardige aandoening na de start van een insuline behandeling wordt gemeld, kan meerdere betekenissen hebben:
1. iedereen is er van overtuigd dat insuline kanker veroorzaakt, en dat dit dus niet meer gemeld hoeft te worden. Ondanks het feit dat insuline eigenlijk in het lichaam een groeifactor is, een anabool hormoon, acht ik dit scenario uitermate onwaarschijnlijk.
2. iedereen is er van overtuigd dat insuline behandeling juist niets met het ontstaan van een tumor te maken heeft. Dit scenario lijkt me niet onwaarschijnlijk, en de conclusie van ‘reverse causation’ van de Eindhovense onderzoekers wijst in die richting. Vraag is dan wel waarom een dergelijke bijwerking wél wordt gemeld bij het gebruik van nieuwere middelen, als GLP1 RA, en niet in het geval van behandeling met insuline. Hier lijkt sprake van rapportage bias, en misschien wel indoctrinatie: “alles melden over nieuwe middelen, de bestaande middelen zijn niet belangrijk om te rapporteren”. En als een tumor wordt vastgesteld (gediagnostiseerd) zo’n 3 maanden na de start van een GLP1 RA, is er waarschijnlijk ook sprake van ‘reverse causation’.
Rare meldingen van bijwerkingen
Het melden van bijwerkingen lijkt overigens een ‘vak op zich’. U zult waarschijnlijk wel weten, dat insuline gebruikt wordt voor de behandeling van diabetes mellitus en verhoogde bloedglucose waarden. Het is dan ook erg bijzonder dat bij het beschouwen van de gerapporteerde bijwerkingen van bovengenoemde insulinesoorten op de website van Lareb blijkt, dat in totaal 25 maal als bijwerking ‘diabetes mellitus’ wordt gerapporteerd, en 86 x als bijwerking ‘hoge bloedsuiker’ (hyperglycemie) wordt gemeld! Heel bijzonder.
Falen op orale middelen
Het is al DECENNIA bekend dat er bij mensen met type 2 diabetes, die falen op orale medicatie en moeten overgaan op insuline, vaak sprake is van een onderliggende aandoening, die dan pas enkele maanden na de switch naar insuline manifest wordt. Bij secundair falen op orale medicatie wordt vaak gescreend op een onderliggende oorzaak zoals schildklierlijden of blaasontstekingen. In de (inter)nationale richtlijnen wordt niet aanbevolen verder op zoek te gaan naar een onderliggende aandoening. Desalniettemin heb ik de afgelopen jaren zelf meerdere patiënten gezien, bij wie de symptomen van alvleesklierkanker, bijvoorbeeld geelzucht of buikpijnklachten, optraden in de eerste 6 maanden na de overstap naar insuline: ‘reverse causation’.
Prospectief onderzoek naar bijwerkingen
Wanneer we het ontstaan van bijwerkingen en neveneffecten van oude middelen als insuline, en nieuwe middelen als GLP1 receptor agonisten op de juiste manier willen beoordelen, dan moeten ALLE mensen die met een dergelijke behandeling starten, worden gevolgd en moeten ALLE bijwerkingen worden gerapporteerd. Al jaren geleden hebben dr. Henk-Jan Aanstoot, kinderarts in Rotterdam, en ik daarvoor gepleit in een artikel in het Tijdschrift voor Diabetologie (u vindt dit hier: https://gmed.nl/PAS2003.pdf). En juist een dergelijke follow-up studie hebben Mehul Dalal et al uitgevoerd, en hun fraaie onderzoek rapporteren zij in het januari nummer van Endocrine Practice (http://www.ncbi.nlm.nih.gov/pubmed/25148821). Vanuit een geïntegreerde gezondheidszorg database vergeleken zij de klinische en economische uitkomsten van patiënten met type 2 diabetes, die met basale insuline en een GLP1 RA werden behandeld, met de uitkomsten van patiënten die behandeld werden met een multipele insuline injecties. Met name is interessant dat zij keken naar specifieke uitkomsten wat betreft aandoeningen van de alvleesklier, vastgesteld als ‘primary or secondary diagnosis of pancreatic disease (ICD-9-CM diagnosis code 577.xx’). En wat bleek? Aandoeningen van de alvleesklier kwamen vaker voor bij de patiënten die werden behandeld met multipele insuline injecties, namelijk bij 1.9%, en slechts bij 1.2% van de patiënten die werden behandeld met een GLP1 RA. Bovendien was de behandeling van basale insuline met een GLP1 RA goedkoper, en geassocieerd met minder ziekenhuisopnames. Nadeel van deze studie is dat het gegevens zijn, die gebaseerd zijn op een database. Specifieke gegevens over andere bestaande aandoeningen (comorbiditeit) waren beperkt beschikbaar, en van slechts 20% van de patiënten waren gegevens over de diabetesregulatie als bv. HbA1c waarden beschikbaar.
Retrospectieve surveillance?
Men kan zich echter voorstellen dat wanneer we in Nederland de handen ineen slaan, het mogelijk moet zijn om van de laatste 5 – 10 jaar alle patiënten, die gestart zijn met insuline, of met een GLP1 RA, na te zoeken hoe hun ziektebeloop was na de start van deze medicatie. Er is veel informatie over dit onderwerp beschikbaar in de klinische dossiers van huisartsen en internisten, maar deze informatie is helaas moeilijk te benaderen of te ontsluiten. Ongetwijfeld kunnen ook hier grote databases van zorgverzekeraars een belangrijke bron van informatie zijn. De dossiers van de gemiddelde huisartspraktijk of specialistenpraktijk zijn waarschijnlijk te ongestructureerd om dit soort gegevens gemakkelijk en via slimme ICT technieken boven water te krijgen.






Recente reacties